パラジウム酸化的付加錯体によるタンパク質修飾
Palladium Oxidative Addition Complexes for Protein Modification
ペプチドやタンパク質などの生体関連分子の化学的修飾,いわゆる生体共役反応は,人工的に生命機能を操作・制御・追跡するための重要な手法である。また,抗体-医薬複合体と呼ばれる次世代医薬品の開発に不可欠な技術であることからも注目を集めている。その実現には,高い官能基選択性・位置選択性および生体適合条件(中性pH,室温程度,水系溶媒)が求められるため,化学反応開発における最先端研究課題といえる。
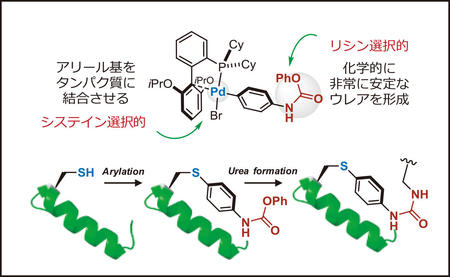
2015年,米国・マサチューセッツ工科大学のB. L. PenteluteとS. L. Buchwaldらはパラジウム酸化的付加錯体を用いたシステイン選択的アリール化反応を報告した1)。この反応は,遷移金属錯体を用いているにもかかわらず,生体適合条件下に効率良く反応が進行し,タンパク質や抗体の修飾への応用も可能である。また彼等は,用いる配位子の構造や反応条件を精査することで,ペプチドのリシン選択的アリール化反応の開発にも成功している2)。さらに2018年,同グループからパラジウム酸化的付加錯体を用いたペプチドおよびタンパク質の選択的クロスリンキング反応3)が報告された。彼等はクロスリンク反応剤として,カルバメートを有するパラジウム錯体を設計・合成し,タンパク質中のシステイン-リシン残基間に安定な架橋構造を構築することに成功した。このようなパラジウム酸化的付加錯体は,多様な官能基をネイティブタンパク質に導入することが可能であり,今後のケミカルバイオロジー分野への幅広い応用が期待される。
1) B. L. Pentelute, S. L. Buchwald et al., Nature 2015, 526, 687.
2) B. L. Pentelute, S. L. Buchwald et al., Angew. Chem. Int. Ed. 2017, 56, 3177.
3) B. L. Pentelute, S. L. Buchwald et al., J. Am. Chem. Soc. 2018, 140, 3128.
久保田浩司 北海道大学大学院工学研究院