酸化的カップリングにおける超原子価ヨウ素触媒法
酸化的カップリングは,炭素-水素結合を直接,官能基化や結合形成に用いるといった点で,グリーンケミストリーに合致した魅力的な合成戦略である。本法に基づく新しい合成法として,芳香環をあらかじめ官能基化することなくカップリングさせる反応が実現し,ここ数年,注目を集めている1),。
筆者らは2008 年に,芳香環に関して優れた選択性を示す超原子価ヨウ素反応剤を用いた,世界初のメタル触媒フリーな新法を報告した2)。この成功を契機に,二量体や過剰酸化のため難しいと思われてきた酸化的クロスカップリングが,様々な基質でうまくいくことが明らかになった。一方,超原子価ヨウ素反応剤の触媒化についての例はなく,その実現には高活性なヨウ素触媒の設計が不可欠であった。
反応開発と並行して行っているヨウ素触媒設計の中で,最近,高い反応性と化学選択性を併せ持つ新規架橋型超原子価ヨウ素種1 を同定した3)。そこで,メタクロロ過安息香酸(mCPBA)を再酸化剤として,これを触媒に用いると,アニリン類と様々な芳香族化合物との酸化的カップリングが効果的に進行することがわかった4)。ここでは触媒1 の使用に加えて,酸化により発生するアニリン環上の正電荷を,アニリン窒素上のアルキルスルホニル(Ms =メシル)酸素原子がn-p*相互作用を通じて安定化することが,重要となる。本法は有機触媒を用いる初のメタルフリーな芳香環酸化的カップリングの例であり,このように超原子価ヨウ素種は,炭素,窒素,酸素などの典型元素から成る有機分子触媒とは性質が大きく異なり,金属元素と近い反応性を示す5)。
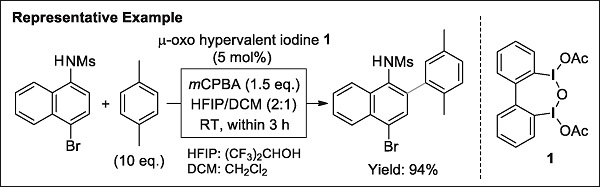
1) 芳香環クロスカップリングの先駆的な例:D. R. Stuart, K. Fagnou, Science 2007, 316, 1172.
2) T. Dohi, Y. Kita et al., Angew. Chem. Int. Ed. 2008, 47, 1301.
3) T. Dohi, Y. Kita et al., Chem. Commun. 2010, 46, 2073.
4) M. Ito, T. Dohi, Y. Kita et al., J. Am. Chem. Soc. 2013, 135, 14078.
5) Y. Kita, T. Dohi, Chem. Rec. 2015, DOI: 10.1002/tcr.201500020.
土肥寿文 立命館大学薬学部創薬科学科