無機酸化物中のヒドリドの性質
Properties of Hydride Ion in Inorganic Oxides
周期表の中で最も単純な原子である水素は,組み合わせる元素や反応条件によって両性元素としてカチオン(プロトン:H+)にもアニオン(ヒドリド:H-)にもなりうる。酸化物にも,水素を含有するものが鉱物を含め多数知られているが,そのほぼすべてはH-ではなくH+として存在する。このような理由から,最近まで酸化物中のヒドリドの性質や振る舞いについては不明な点が多かった。
近年では金属水素化物を用いたトポケミカル反応や高圧合成法により新規の酸水素化物(ヒドリドを含む酸化物)が次々と報告されている。新たに合成された酸水素化物は,単に物質のレパートリーを増やしただけではなく,ヒドリド伝導1)やトポケミカル反応の前駆体としての利用2),アンモニア触媒活性3)など酸化物には見られない興味深い機能が発現することがわかってきた。
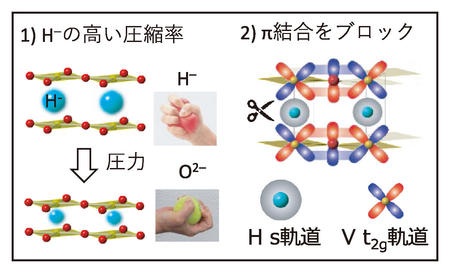
筆者らは,酸化物イオンとヒドリドが層状に秩序化した酸水素化物SrVO2H の圧力下の振る舞いを調べることによってヒドリドの2つの新たな性質を明らかにした(図)4)。1つはヒドリドが酸化物イオンに比べ2倍以上圧縮されやすいという性質である。もう1 つはヒドリドがp軌道を持たないことから,π 結合できない性質である。この性質によりSrVO2Hは擬二次元的な電子構造をとり,超高圧下で特異な圧力誘起金属-絶縁体転移を起こす。これらの性質を巧みに利用することができれば,アニオン秩序構造の制御や,軌道の対称性を利用した革新的な次元性制御など,これまでにない無機化合物の物質設計が可能になる。
1) G. Kobayashi et al., Science 2016, 351, 1314.
2) T. Yajima et al., Nat. Chem. 2015, 7, 1017.
3) Y. Kobayashi et al., J. Am. Chem. Soc. 2017, 139, 18240.
4) T. Yamamoto et al., Nat. Commun. 2017, 8, 1217.
山本隆文 東京工業大学フロンティア材料研究所