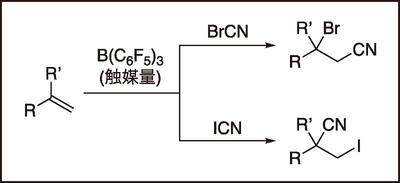
ハロ官能基化反応の位置選択性
Regioselectivity in Halofunctionalizations
塩素や臭素を用いるアルケンのジハロゲン化反応は,2つのハロゲノ基を分子内に導入するための古典的な有機反応である。それに対して,ハロゲノ基とほかの官能基を1つずつ導入する反応,すなわちハロ官能基化反応が近年精力的に開発されている。ハロ官能基化反応を考える上で重要となるのが,位置選択性(どちらの炭素にハロゲンが付加するか)である。不要な位置異性体の生成は,目的生成物の収率の低下や分離コストの増加によるEファクター1)の増大に繋がる。言い換えれば,所望の位置異性体を選択的に合成することがグリーンケミストリーにおいては重要となる。
2023年に清川・南方らは,BrCNを用いるアルケンのシアノブロモ化反応を報告した2)。触媒量のB(C6F5)3を添加することで反応が促進されることを見いだし,一方の位置異性体を選択的に合成することに成功した。同年に荒井らはICNを用いるアルケンのヨードシアノ化反応を報告した。本報告においてもB(C6F5)3が優れた触媒活性を示すが,興味深いことに,シアノブロモ化反応とは異なる位置選択性が発現した。これについて荒井らは,BrCNとICNのハロゲン上のσ-ホール(原子の表面に生じる正電荷)の大きさの差によって,位置選択性の違いが説明可能であることを見いだしている。詳しくは文献3)を参照されたい。
今回紹介した2つの反応を見比べると,ハロゲンの種類を変えることによって,位置選択性が制御可能であることがわかる。位置選択性のユニークな逆転現象が有機化学の深い理解に繋がった一例であり,他のハロ官能基化反応への波及効果も期待される。
1) R. A. Sheldon, Green Chem. 2007, 9, 1273.
2) K. Kiyokawa, I. Noguchi, T. Nagata, S. Minakata, Org. Lett. 2023, 25, 2537.
3) I. Furusawa, T. Suzuki, Y. Yu, T. Arai, Adv. Synth. Catal. 2023, 365, 3247.
大村修平 名古屋大学大学院工学研究科