分子集合が創発する励起状態が切り拓く光医療の新展開
Emergent Excited States Generated by Molecular Assemblies: Opening a New Frontier in Photomedicine
光線力学療法(Photodynamic therapy; PDT)は,光増感剤が光を吸収し,励起状態を経て生成する活性酸素種やラジカル種が病巣を破壊することで治療効果を発揮する光医療として発展してきた。またPDTは,病巣破壊にとどまらず,細胞死に伴う免疫原性の変化を介して,生体が本来有する免疫応答を活性化し得ることも示されている1)。PDTの鍵となるのは,光吸収後に生成する三重項状態や電荷分離状態であり,これらは治療効果を生み出す光化学反応において中心的な役割を担っている。近年では,PDTの反応様式や時間スケールが免疫系との相互作用に影響を与える可能性が示唆されており,免疫活性化の観点から治療効果を高めようとする潮流が広がっている。
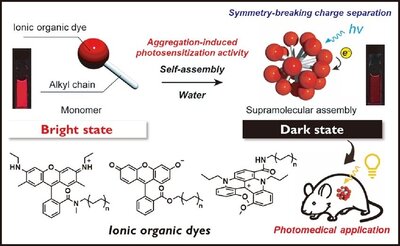
筆者らは,イオン性有機色素分子の集積により生じる光誘起対称性破壊型電荷分離(Symmetry-breaking charge separation; SB-CS)によって形成される電荷分離状態が,高いPDT活性につながることを見いだした2, 3)。さらに,この分子集合誘起SB-CSをレドックス活性なイオン性有機色素に適用することで,その集合体が細胞内部で持続的な酸化還元反応を引き起こし,腫瘍内部の低酸素環境下においても優れたPDT効果を示すことを明らかにした4)。本手法は,免疫系に作用する治療戦略とも親和性が高く,分子集合が創発する励起状態はPDTを「生体応答を引き出す医療」へと進化させる新たな基盤となることが期待される。
1) Y. Cai et al., Signal Transduct. Target. Ther. 2025, 10, 115.
2) H. Shigemitsu et al., Chem. Sci. 2020, 11, 11843.
3) H. Shigemitsu et al., JACS Au 2022, 2, 1472.
4) Y. Imuro et al., ChemRxiv, 2026. doi: 10.26434/chemrxiv.10002016/v1
重光 孟 国立研究開発法人物質・材料研究機構(NIMS)高分子・バイオ材料研究センター